 Sauerstoff 2 Sauerstoff 2
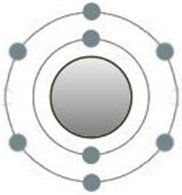
Im Kfz-Bereich kennt man Sauerstoff z.B. bei Oldtimern von seiner unangenehmen Seite, wenn Rost in allen Teilen die Form einer Karosserie langsam aufl÷st. Man sandstrahlt und fast nichts bleibt ³brig, an das
man ankn³pfen k÷nnte. Dass nicht nur der Sauerstoffanteil der Luft, sondern auch noch deren Feuchtigkeitsanteil eine Rolle spielt, erlebt man spõtestens, wenn man ein altes Auto aus Kalifornien importiert.
Reiner Sauerstoff kann also sowohl aus der Luft als auch dem Wasser gewonnen werden, letzteres allerdings durch Elektrolyse mit mehr Energieaufwand. Die Reaktion beim Rosten von Eisen-Metallen haben ihre
Ursache aber nicht so sehr in den Sauerstoffatomen des Wassers selbst, sondern werden eher durch den im Wasser gel÷sten Sauerstoff verursacht.

Aus fl³ssigem Roheisen kann man mit Hilfe von Sauerstoff Stahl gewinnen. Das Bild zeigt ³brigens den
ersten Tiegel des Sauerstoff-Aufblasverfahrens, mit dem das gelang. Mit dem zweiten Tiegel begann 1952/53 in Linz die Produktion, kurz danach wurde das zweite Stahlwerk in Donawitz in Betrieb genommen. Das
Verfahren wird alternativ auch nach dem Namen der beiden Standorte benannt.
Der Tiegel war feuerfest ausgemauert, enthielt bis zu 30 Tonnen fl³ssiges Roheisen, in die durch eine wassergek³hlte Lanze mit etwa 10 bar im Abstand von 30 bis 100 cm reiner Sauerstoff geblasen wurde. Auch
als 'Frischen' bekannt, entstehen hohe Temperaturen, die den Anteil von Kohlenstoff senken. Weitere unerw³nschte Bestandteile wie Phosphor und Schwefel verbrennen ebenfalls. Der Einblasvorgang kann auch
vom Boden des Tiegels erfolgen.
Wer noch mit Acetylen geschwei▀t hat, kennt Sauerstoff in alten, blauen Stahlflaschen mit ca. 150 bar Druck. Der Sauerstoff verbrennt zwar selbst nicht, ist aber f³r die gro▀e Hitze verantwortlich, die Stahl zum
Schmelzen bringt. Was in normaler Luft schon fast abgebrannt ist, wird in reinem Sauerstoff noch einmal hell auflodern.
Weil solche Effekte selbst bei nur erh÷htem Sauerstoffanteil in der Luft auftreten k÷nnen, muss alles Brennbare aus der Nõhe einer Sauerstoffquelle entfernt werden. ųl oder Fett an der Verschraubung von
Sauerstoffflaschen k÷nnen fast explosionsartig verbrennen. Umgekehrt f³hrt eine schnelle Entleerung einer solchen Flasche u.U. zu Eisbildung.
Und trotzdem bezeichnen wir den Antrieb f³r noch fast alle unsere Fahrzeuge als Verbrennungs- und nicht als Explosionsmotor. Das liegt daran, dass Sauerstoff zwar zusammen mit allen m÷glichen Stoffen, darunter
die schon erwõhnten Metalle, ein Oxid bildet, die Reaktionen aber bei Raumtemperatur vergleichsweise langsam verlaufen.
Alleine gibt es Sauerstoff nõmlich nur als O2-Molek³l und diese Verbindung muss erst aufgespalten werden, bevor sich einzelne O-Atome mit anderen Stoffen verbinden k÷nnen. Typisch f³r eine
Verbrennung ist auch die Menge an Wõrmeenergie, die erst einmal eingesetzt werden muss, um dann von selbst sehr viel mehr Energie in Form deutlich steigender Temperaturen zu liefern.
Zu den Besonderheiten der Reaktion von Sauerstoff mit Stickstoff lesen sie bitte im nõchsten Kapitel weiter . . .
|